글자크기 설정
기사의 본문 내용은 이 글자크기로 변경됩니다.
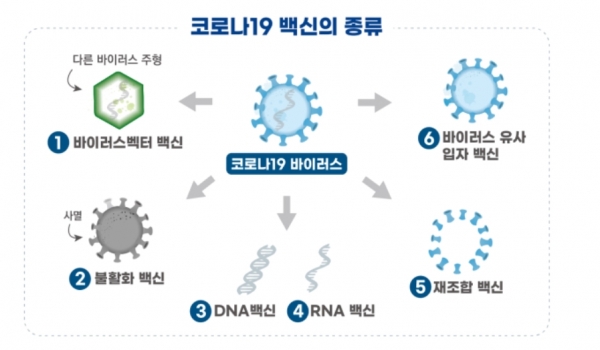
[서울파이낸스 김현경 기자] 식품의약품안전처는 아이진이 개발하는 코로나19 백신 후보물질 이지 코비드(EG-COVID)의 임상 1·2a상 시험 계획을 승인했다고 31일 밝혔다. 임상 1·2a상이 동시에 승인된 데 따라 아이진은 1상에서 안전성을 확인한 뒤 2a상시험을 할 예정이다.
이지 코비드는 코로나19 바이러스의 표면항원 단백질 정보를 담은 메신저 리보핵산(mRNA) 백신이다. 코로나19 바이러스 항원 정보를 가진 유전자를 mRNA 형태로 주입해 체내에서 항원 단백질을 합성하고, 이 항원 단백질이 면역세포를 자극해 바이러스를 무력할 수 있는 중화항체 생성을 유도한다. 백신 접종 후 바이러스가 인체에 침입했을 때 바이러스를 중화하는 방식으로 제거한다. mRNA의 세포 내 전달을 위한 물질로는 리포솜이 사용됐다.
식약처는 "코로나19 치료제·백신 개발을 지원해 국민이 질병을 예방하고 치료 기회를 보장받을 수 있도록 최선을 다하겠다"고 했다. 한편, 이번 이지 코비드 승인으로 국내에서 코로나19와 관련된 임상시험 건은 백신 11개, 치료제 13개(12개 성분)가 됐다.
이 기사를 공유합니다
관련기사
- 진매트릭스, 코로나19 변이 진단키트 국내 허가 획득
- 식약처 "코로나 백신 요약보고에 이상사례·안전성 포함해야"
- 국가임상지원재단, SK바사 백신 임상 참여하면 인센티브
- 식약처, 코비박 코로나19 백신 사전검토 착수
- 툴젠, 엠큐렉스와 mRNA 유전자치료제 공동개발
- 국가임상지원재단, 코로나19 백신 임상참여 사이트 개설
- 에스티팜, 테라젠바이오와 mRNA 항암백신 개발 협약
- 셀트리온, 차세대 mRNA 백신 플랫폼 개발 착수
- 고혈압약서 불순물 초과 검출···식약처 "인체 위해 우려 낮아"
- 위드마스크에 감염병 감소세···독감백신 필수일까
- 국가임상재단, 국산 코로나19 백신 임상 희망자 723명 연계
- 추석연휴 응급상황 대처법은?
- 부광약품, '레보비르' 코로나19 치료제 개발 중단











![[광명소식] 보건복지부 '그냥드림' 시범사업장 선정 등](https://cdn.seoulfn.com/news/thumbnail/custom/20251126/613704_413206_721_1764122841_220.jpg)
