글자크기 설정
기사의 본문 내용은 이 글자크기로 변경됩니다.
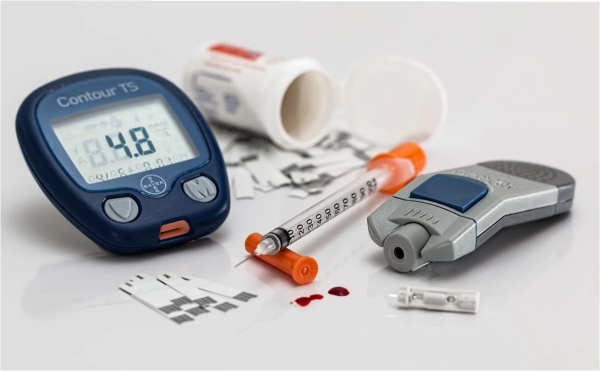
[서울파이낸스 김현경 기자] 앞으로 임신테스트기, 혈당측정기를 비롯한 체외진단의료기기는 사용 목적과 위해성 정도에 따라 4개 등급으로 분류해 관리된다.
식품의약품안전처는 27일부터 내년 1월6일까지 체외진단의료기기의 특성에 맞는 허가·관리체계를 주요 내용으로 하는 체외진단의료기기법 시행령 및 시행규칙 제정안을 입법예고한다고 밝혔다.
주요 내용은 등급 분류 기준 마련과 인허가 및 심사 절차 규정, 임상적 성능시험기관 지정 및 실시기준 마련, 임상검사실 체외진단검사 기준 도입이다.
식약처는 체외진단의료기기의 등급은 사용 목적과 잠재적 위해성 정도에 따라 4개 등급으로 분류하고, 식약처장이 세부 품목별로 등급을 정해 고시하도록 했다. 인허가 및 심사 절차는 원재료나 사용 목적처럼 중요사항이 변경된 경우에만 변경허가를 받고, 이외의 변경사항에 대해서는 단순 보고만 하도록 절차를 규정했다.
혈액, 체액 같은 검체를 이용하는 체외진단의료기기의 경우 임상적 성능시험을 실시하는 기관의 시설, 인력 기준을 마련했다. 임상검사실의 체외진단검사 인증을 받으려면 인증 신청서에 품질관리체계, 전문인력의 숙련도에 관한 자료를 첨부해 식약처장에게 신청하도록 하는 기준도 도입했다.
식약처는 "이번 제정안을 통해 체외진단의료기기의 특성을 고려한 허가·관리 체계가 마련돼 체외진단기기에 대한 연구개발 및 제품화를 촉진할 것으로 기대한다"고 설명했다.
이 기사를 공유합니다
관련기사
- 차바이오텍, 폐암세포 분리·배양 방법 국내 특허 획득
- 식약처, 세포·유전자치료제 심사 강화
- 동국생명과학, 바이엘 안성공장 사들여 수출 확대 포석
- '혁신신약' 특허심사, 평균 11개월 빨라진다
- GC녹십자엠에스, 인도에 당화혈색소측정시스템 수출
- 스포츠·마사지 화장품 온라인 광고 33% '허위·과대'
- GC녹십자엠에스, 인플루엔자 진단기술 미국특허 획득
- 식약처, 가상현실 적용 의료기기 평가 기술 개발
- 식약처, 테스토스테론 검출 단백질 보충제 통관차단 요청
- [새해 달라집니다-식품·의약품] 커피 카페인 표시·마약사범 교육 의무
- 식약처, AI 기반 암진단 소프트웨어 첫 허가
- 국내 의료기기 생산액 7조원 돌파···임플란트 3년 연속 1위
- GC녹십자의료재단, 체외진단의료기기 성능시험기관 지정


![[에너지탄소포럼] 강민구 변호사 "한국 VCM, 지원 중심 입법이 시급"](https://cdn.seoulfn.com/news/thumbnail/custom/20251126/613709_413212_059_1764126061_220.jpg)








![[광명소식] 보건복지부 '그냥드림' 시범사업장 선정 등](https://cdn.seoulfn.com/news/thumbnail/custom/20251126/613704_413206_721_1764122841_220.jpg)
