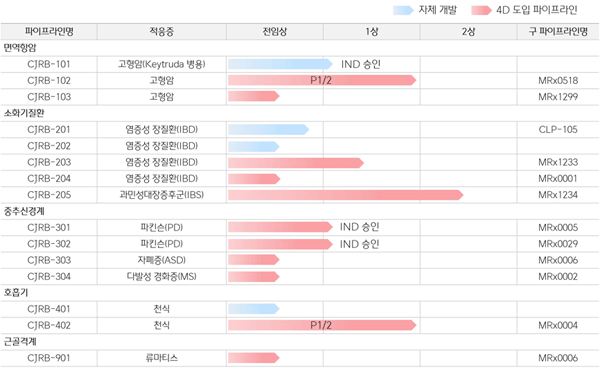
[서울파이낸스 김혜지 기자] 씨제이(CJ)제일제당의 제약 독립법인 CJ바이오사이언스가 마이크로바이옴(미생물 생태계) 신약 파이프라인(후보 물질)을 15개로 확정했다. 25일 CJ제일제당에 따르면, CJ바이오사이언스의 신약 파이프라인 가운데 4개가 자체 개발이고, 나머지는 모두 영국·아일랜드 소재 신약 개발 기업 포디파마(4D Pharma)로부터 인수했다.
CJ바이오사이언스는 지난 3월 4D파마의 후보 물질 인수 뒤 분석에 나섰다. 그 결과 개발 성공 가능성이 큰 후보 물질 중심으로 신약 파이프라인 분류를 끝냈다. 후보 물질과 함께 확보한 유럽인 장내 마이크로바이옴 관련 자료를 토대로 독자 균주 자료관(라이브러리)과 자료 뭉치(데이터베이스)를 만들어 신약 개발에 힘쓸 방침이다.
CJ바이오사이언스는 지난해 1월 출범 당시 발표한 '2025년까지 파이프라인 10건 확보' 목표를 2년 이상 앞당기게 됐다. 확정한 파이프라인 가운데 주력은 경구투여 항암제로 개발하는 'CJRB-101'이다.
비소세포폐암과 두경부편평세포암종처럼 고형암이 적응증인 CJRB-101은 자체 항암 효능을 가졌다. CJRB-101 단독 투여했을 때 항암 효능이 면역항암제 '키트루다'(성분명 펨브롤리주맙)와 함께 투여할 경우보다 뛰어난 것으로 확인됐을 정도다.
CJ바이오사이언스는 국내 식품의약품안전처와 미국 식품의약국(FDA)에 CJRB-101에 대한 임상 1·2상 계획(IND)을 승인받았다. 올해 9월부터 환자를 모집해 2025년 상반기까지 임상 1상을 마무리하고 2상에 돌입할 계획이다. 조병철 연세대학교 의과대학 종양내과 교수(연세암병원 폐암센터장)가 한국과 미국 임상을 주도한다.
CJ바이오사이언스 쪽은 "글로벌 제약사(빅파마)에서도 CJRB-101을 비롯한 여러 파이프라인에 관심을 보이고 있다"며 "임상 파이프라인 숫자는 신약 개발 기업의 경쟁력 지표로 여겨지기 때문에 지속 성장 발판을 마련하게 된 셈"이라고 했다.


